מחלת אלצהיימר, הפרעה נוירודגנרטיבית מתקדמת המשפיעה על כ-55 מיליון אנשים ברחבי העולם, מובילה לירידה קוגניטיבית חמורה ואובדן זיכרון. חוקרים ממכון אוקינאווה למדע וטכנולוגיה פיתחו פפטיד סינתטי, PHDP5, המכוון לאלצהיימר בשלב מוקדם על ידי הבטחת זמינות הדינמין למחזור שלפוחית עצבים בנוירונים, תוך הדגמה של שיקום משמעותי של פונקציות זיכרון ולמידה בעכברים מהונדסים.
הוכח כי טיפול חדש נלחם ביעילות בירידה קוגניטיבית בעכברים עם מחלת אלצהיימר.
אלצהיימר מחלה, הפרעה נוירודגנרטיבית מתקדמת, עומדת כגורם העיקרי לדמנציה. מצב זה מוביל להידרדרות קוגניטיבית, אובדן זיכרון, ובסופו של דבר גורם לאנשים לא להיות מסוגלים לבצע פעולות יומיומיות. נכון לעכשיו, הוא משפיע על כ-55 מיליון אנשים ברחבי העולם. ביפן, כ-4.4 מיליון אנשים סובלים מדמנציה, עם תחזיות המצביעות על כך שהנתון הזה יעלה ל-6.5 מיליון עד 2060, על פי נתונים סטטיסטיים של הממשלה.
ריפוי או דחיית הסימפטומים המתישים של אלצהיימר הוא קשה במיוחד בשל האופי החמקמק של המחלה. הסיבה המדויקת אינה ידועה, וככל הנראה כרוכה במספר גורמים מגנטיקה ועד אורח חיים, ובשל האופי המתקדם של המצב, לעתים קרובות מאוחר מדי לטפל ביעילות ברגע שהתסמינים מתחילים להשפיע על חיי היומיום.
עם זאת, צוות חוקרים מהיחידה לשעבר לתפקוד סלולרי ומולקולרי במכון למדע וטכנולוגיה באוקינאווה (OIST), בראשותו של פרופסור אמריטוס טומויוקי טקהאשי, התקדם כעת במציאת טיפול בר-קיימא לתסמינים הללו, והדביק אותנו. הדרך להצלת תפקודי מוח לפני שהם ייפגעו באופן בלתי הפיך על ידי מחלת האלצהיימר. הממצאים שלהם פורסמו לאחרונה ב חקר המוח. "הפכנו בהצלחה את הסימפטומים של מחלת אלצהיימר בעכברים", מסביר ד"ר צ'יה-ג'ונג צ'אנג, מחבר המחקר הראשון וכיום חבר ביחידה לחישוב עצבי ב-OIST. "השגנו זאת עם פפטיד קטן וסינטטי, PHDP5, שיכול לחצות בקלות את מחסום הדם-מוח כדי לכוון ישירות למרכז הזיכרון במוח."
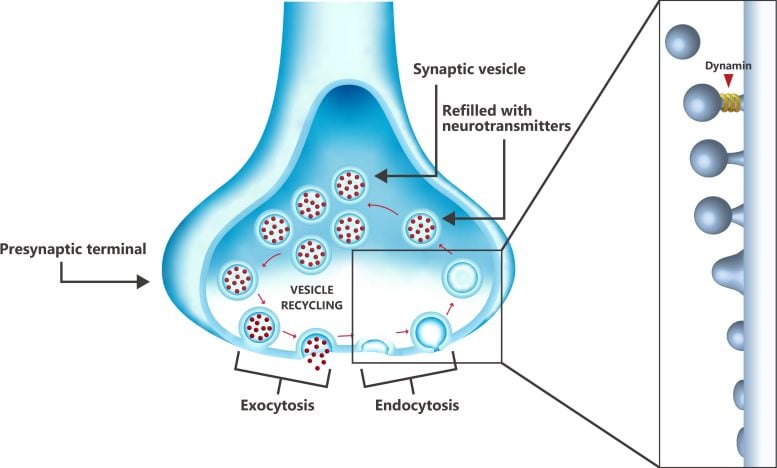
מיחזור שלפוחית במסוף הפרה-סינפטי בקצה אחד של נוירון, המראה את תפקיד הדינמין בשלב האחרון של האנדוציטוזיס (החזרת ממברנה), שבו החלבון מנתק את השלפוחית מקרום התא. לאחר מכן ממלאים את השלפוחית בנוירוטרנסמיטורים ומועברת חזרה לאתר השחרור של קרום התא, שם משתחררים הנוירוטרנסמיטורים, והשלפוחית ממוחשבת. קרדיט: Kaori Serakaki/OIST
חיסכון בדינמין
גורם מרכזי במחלת אלצהיימר הוא בריאות הסינפסות המוחיות. סינפסות הן הצמתים בין נוירונים במוח, שבהם המידע מועבר מנוירון אחד למשנהו באמצעות נוירוטרנסמיטורים כימיים העטופים בשלפוחיות סינפטיות. יש למחזר את השלפוחיות הללו כל הזמן כדי להבטיח אספקה קבועה, ושלב חיוני בתהליך מיחזור השלפוחית הוא שליפת הממברנה (אנדוציטוזיס) על ידי החלבון דינמין, אשר 'חותך' את השלפוחית מקרום התא. דינמין זמין בכל הנוירונים, בחופשיות או קשורה למיקרו-צינוריות המרכיבות את שלד הציטוס של התאים.
האנטגוניסט המרכזי כאן הוא החלבון טאו, שבנסיבות רגילות מעורב בייצוב המיקרוטובולים. עם זאת, בשלב המוקדם של אלצהיימר, הטאו מתחיל להתנתק ממיקרוטובולים. בהיותו זמין בחופשיות, טאו מרכיב יתר על המידה מיקרוטובוליות חדשות, שואב ביעילות את הדינמין מהתא, מה שהופך אותו ללא זמין לשלב האחרון של האנדוציטוזיס. ככל שהאלצהיימר מתקדם, הטאו המצטבר מתקבץ לסבכים נוירו-פיברילריים, שהם סימן ההיכר של המחלה – עד שהסבכים האלה מופיעים בסריקות מוח, לעתים קרובות מאוחר מדי לטפל במחלה.
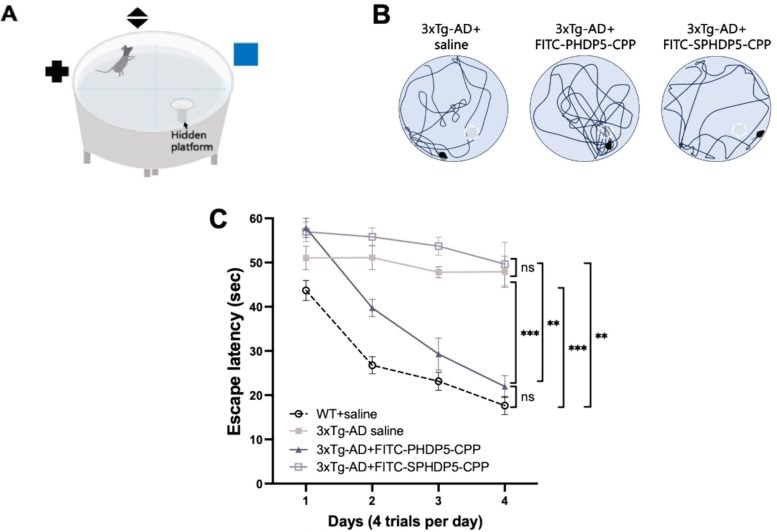
כמה מהממצאים העיקריים מהעיתון. SPHDP5 הוא פפטיד מקושקש שאין לו השפעה טיפולית, המשמש כבקרה. א) מציג את מערך הניסוי עם מבוך מים של מוריס, לפיו מכניסים עכבר לאמבט מים ומאומנים למצוא פלטפורמה נסתרת באמצעות רמזים חזותיים. ב) הם איורים מייצגים של שבילי השחייה של העכברים לעבר הפלטפורמה הנסתרת (קו לבן מקווקו). ג) מראה את ההשפעה של מתן תוך-אף של PHDP5 לאורך זמן – שימו לב כיצד העקומות של עכברים בריאים (קו שחור מקווקו) ועכברים מהונדסים שטופלו ב-PHDP5 (קו אפור עם משולשים) דומות מאוד. קרדיט: Chang et al.
חוקרי ה-OIST התמקדו במיוחד באינטראקציה בין דינמין למיקרוטובולה, והם הוכיחו בעבר את ההשפעות החיוביות של עיכוב אינטראקציה זו במבחנה באמצעות הפפטיד הסינטטי PHDP5. ד"ר זכרי טאאופיק, כיום ביחידה לביולוגיה של סינפסה ב-OIST ומחבר שני של המאמר, מסביר: "על ידי מניעת האינטראקציה בין דינמין למיקרוטובולים, PHDP5 מבטיח שדינמין זמין עבור אנדוציטוזיס שלפוחית במהלך המיחזור, מה שיכול לשחזר את התקשורת האבודה בין נוירונים בתוך הסינפסות בשלב מוקדם."
באמצעות עכברים מהונדסים, החוקרים הראו כעת את אותה השפעה משקמת in vivo. "היינו נרגשים לראות ש-PHDP5 הציל באופן משמעותי את ליקוי הלמידה והזיכרון בעכברים", אומר ד"ר צ'אנג. "הצלחה זו מדגישה את הפוטנציאל של מיקוד האינטראקציה דינמין-מיקרוטובולה כאסטרטגיה טיפולית למחלת אלצהיימר."
מכיוון ש-PHDP5 מעכב אינטראקציות בין דינמין למיקרוטובולות באופן כללי, החוקרים שינו את הפפטיד כך שיכלול פפטיד חודר תאים, המאפשר מתן הטיפול דרך חלל האף שבו מחסום הדם-מוח אינו מפותח במלואו, ואשר קרוב ל- מרכז הזיכרון של המוח, ההיפוקמפוס. בדרך זו, הפפטיד יימסר להיפוקמפוס בריכוז גבוה יותר מאשר באמצעות שיטות מתן אחרות, תוך מזעור תופעות לוואי אפשריות במקומות אחרים בגוף.
ממולקולות ומבוכים ועד לטיפולים ברי קיימא
בתנאי שהסינפסות מטופלות ב-PHDP5 בשלב מוקדם יחסית, ניתן להפוך את הנזק שנגרם על ידי האינטראקציה המשתוללת בין דינמין למיקרוטובולה עד כדי כך שלעכברים הטרנסגניים המטופלים יש יכולות למידה וזיכרון בדומה לעכברים בריאים. בעוד שהפפטיד אינו יכול לרפא אלצהיימר, העיכוב של האינטראקציה בין דינמין למיקרוטובולה מעכב את הירידה הקוגניטיבית באופן משמעותי, עד לנקודה שבה היא עשויה שלא להשפיע על אנשים בריאים באורך חיים נורמלי.
מחוזקים מתוצאות אלו, צוות המחקר, בראשותו של ד"ר טאאופיק ומורכב ממומחים מיחידות שונות ברחבי OIST, ממשיך בעבודתם על הטיפול. ד"ר טאאופיק, שבסיסה ביחידה לביולוגיה של סינפסה, פועלת לשיפור הפפטיד עצמו והדרכים שבהן הוא פועל in vivo. "אנחנו רוצים להגדיל את כמות ה-PHDP5 במוח כדי להשיג אפקטים טובים יותר, תוך מזעור תופעות הלוואי", כדבריו. בינתיים, ד"ר צ'אנג, המבוסס ביחידה לחישובים עצביים, פועל להחדרת AI במרדף אחר נתונים נוספים וחזקים יותר: "אנו משתמשים בתחומי המומחיות השונים בתוך OIST כדי לשפר את המחקר שלנו."
במקביל, הצוות עובד עם חטיבת החדשנות של OIST כדי להעביר את הפפטיד דרך צינור הייצור. "אנחנו רוצים לערב חברות תרופות בעתיד", מסביר ד"ר טאאופיק. "יש להם את המומחיות הדרושה בפרמקולוגיה ואת היכולת לניסויים בבני אדם להפוך את הפפטיד שלנו לטיפול בר קיימא."
בעוד המסע ממחקר לתרופה הוא ארוך לשמצה, ולוקח בממוצע 20 שנה מהנייר למרשם, החוקרים נותרו נלהבים מאוד. כפי שאומר ד"ר צ'אנג, "חיסון הקורונה הראה לנו שניתן לפתח טיפולים במהירות, מבלי לוותר על הקפדה מדעית או על בטיחות. אנחנו לא מצפים שזה יעבור כל כך מהר, אבל אנחנו יודעים שממשלות – במיוחד ביפן – רוצות לטפל במחלת האלצהיימר, שמשפיעה על כל כך הרבה אנשים. ועכשיו, למדנו שאפשר להפוך את הירידה הקוגניטיבית ביעילות אם מטפלים בשלב מוקדם".
הערה מאת OIST פרופסור אמריטוס Tomoyuki Takahashi
בעודו כעת בדימוס מ-OIST, פרופ' טקאהאשי החל את הפרויקט וניהל אותו עד לסגירת היחידה. "במחקר זה, יחד עם הקודם, הבהרנו את המשמעות הפתולוגית של אינטראקציה בין דינמין-מיקרוטובול (MT) במחלת אלצהיימר (AD), שבאמצעותה נפגעים תפקודים סינפטיים באופן משמעותי. מעכב ה-Dynamin-MT PHDP5 מציל חוסר תפקוד סינפטי שנגרם מהצטברות טאו בפרוסות מוח ויכול להפוך למידה וחסרי זיכרון לרמות נורמליות בדגמי עכברי AD מהונדסים. אפקט זה in vivo חזק מכיוון שהוא ניתן לשחזור בבדיקות כפול סמיות ועקבי בשני סוגים של עכברי מודל. ברור שהשלב המכריע הבא הוא הגשת PHDP5 למבחני שלב 1-4 של ניסויים טיפוליים AD, שיבוצעו בצורה הטובה ביותר על ידי חברות תרופות. אנו מקווים מאוד שהפפטיד שלנו יוכל לעבור את הבדיקות ולהגיע לחולי אלצהיימר ללא עיכוב רב ולהציל את הסימפטומים הקוגניטיביים שלהם, שהם הדאגה העיקרית של החולים ובני משפחותיהם".
המחקר מומן על ידי אוניברסיטת אוקינאווה למדע וטכנולוגיה.

